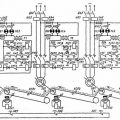
Аккумуляторы – это устройства, которые используются для хранения и поставки электрической энергии. Они являются частью многих электрических устройств, таких как мобильные телефоны, ноутбуки, автомобили и многое другое. Аккумуляторы работают по принципу электрохимической реакции.
Основными элементами аккумулятора являются анод, катод и электролит. Анод – это положительный электрод, а катод – отрицательный. Между ними находится электролит, который служит для перемещения ионов внутри аккумулятора. На поверхностях анода и катода находятся химические вещества, способные вступать в реакцию, связанную с передачей электрических зарядов.
Когда аккумулятор заряжен, химические реакции протекают в обратном направлении: электролит позволяет перемещаться ионам в аккумуляторе, превращая химическую энергию обратно в электроэнергию. Во время разрядки аккумулятора, химическая реакция происходит в прямом направлении, и электроны перемещаются через проводник внешней цепи, создавая электрический ток.
Важно отметить, что аккумуляторы имеют ограниченный ресурс работы и со временем теряют свою емкость. Емкость аккумулятора показывает, сколько электрического заряда он способен хранить. Поэтому аккумуляторы регулярно нуждаются в замене или перезарядке.
Существует много различных типов аккумуляторов, каждый из которых имеет свои особенности и применение. Некоторые из наиболее распространенных типов аккумуляторов включают свинцово-кислотные, никель-кадмиевые, никель-металл-гидридные и литий-ионные аккумуляторы. Каждый из этих типов аккумуляторов обладает своей уникальной структурой и параметрами работы, что определяет их применение в различных областях.
Аккумуляторы являются важным элементом современной техники и повсеместно используются в нашей повседневной жизни. Они обеспечивают бесперебойную работу устройств и удобство использования портативных электронных устройств. Поэтому знание о том, как устроены и работают аккумуляторы, является важным для понимания принципов работы и выбора наиболее подходящего типа аккумулятора для конкретных нужд.
Виды аккумуляторов

1. Свинцово-кислотные аккумуляторы: это наиболее распространенный вид аккумуляторов, который используется в автомобилях, ноутбуках и других устройствах. Они основаны на реакции химических веществ свинца и серной кислоты.
2. Литий-ионные аккумуляторы: такие аккумуляторы обычно используются в современных смартфонах, планшетах и портативных компьютерах. Они обладают высокой энергоемкостью и долгим сроком службы, но требуют осторожного обращения и специального зарядного устройства.
3. Никель-кадмиевые аккумуляторы: эти аккумуляторы широко применяются в портативных электроинструментах и устройствах, таких как фотокамеры и видеокамеры. Они обладают хорошей энергоемкостью и способны выдавать высокий ток, но требуют правильной зарядки для предотвращения эффекта памяти.
4. Никель-металл-гидридные аккумуляторы: такие аккумуляторы широко используются в портативных электронных устройствах, включая фонари, игрушки и беспроводные наушники. Они обладают высокой энергоемкостью, не содержат токсичных веществ и являются более экологически чистым вариантом, чем никель-кадмиевые аккумуляторы.
5. Литий-полимерные аккумуляторы: такие аккумуляторы часто используются в устройствах с низким энергопотреблением, таких как гаджеты и электронные часы. Они обладают высокой энергоемкостью, но могут иметь более низкую устойчивость и безопасность по сравнению с другими типами аккумуляторов.
6. Солнечные аккумуляторы: это особый тип аккумуляторов, которые питаются от солнечной энергии. Они широко применяются в солнечных батареях и других устройствах, которые нуждаются в независимом источнике питания. Солнечные аккумуляторы могут быть выполнены на основе различных химических соединений, включая свинец, кадмий и литий.
Щелочные аккумуляторы
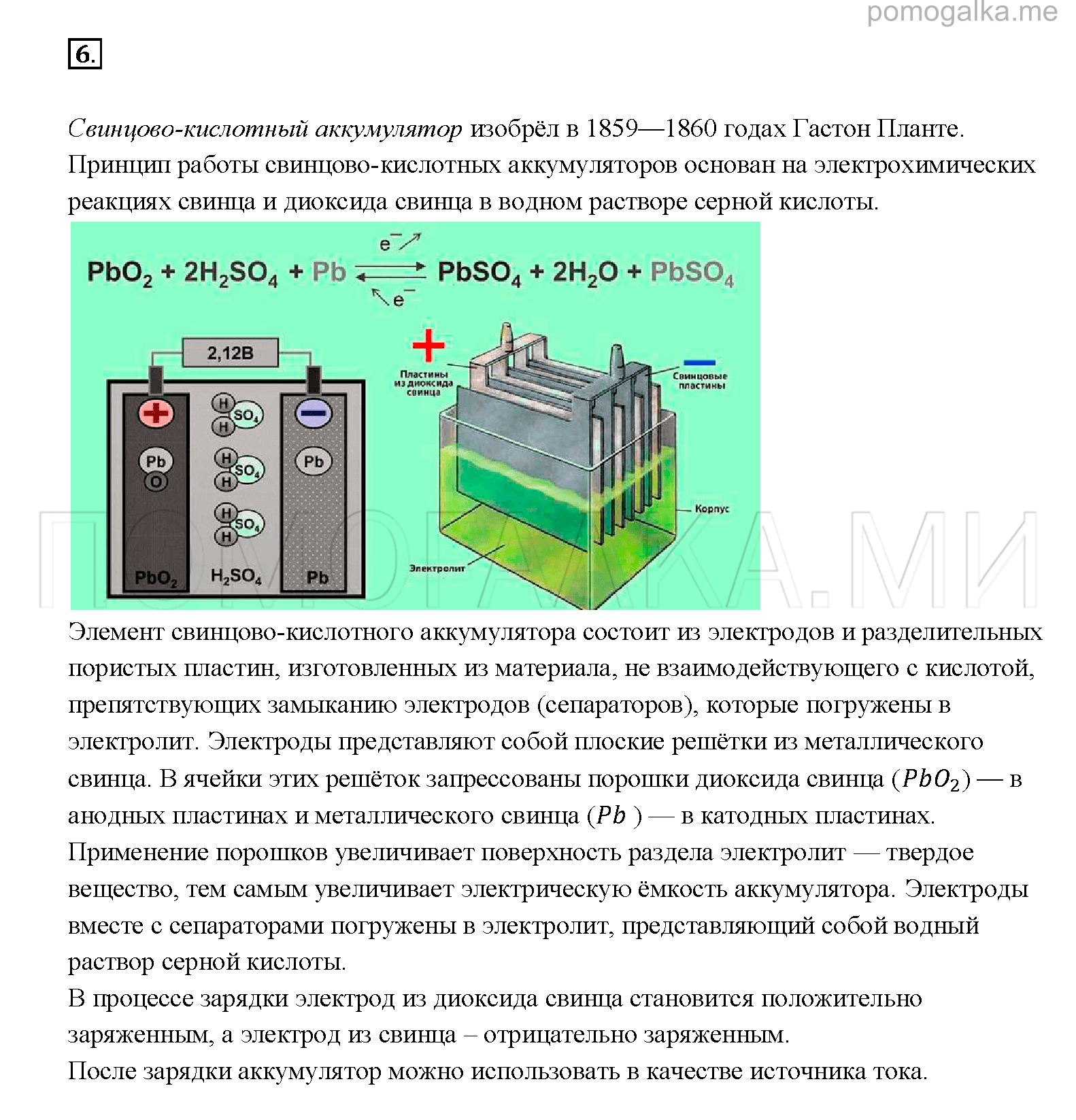
Щелочные аккумуляторы представляют собой одни из самых распространенных типов аккумуляторов, которые широко применяются в бытовых устройствах и электронике.
Они относятся к второму поколению аккумуляторов и обладают преимуществами по сравнению с первым поколением аккумуляторов, такими как никель-кадмиевыми (NiCd) аккумуляторами.
Щелочные аккумуляторы имеют большую ёмкость, что позволяет им работать значительно дольше без подзарядки. Они также обладают малым саморазрядом, что означает, что они могут длительное время хранить энергию без потери.
Эти аккумуляторы могут быть заряжены и разряжены множество раз, что делает их более экономичными и долговечными. Они также не содержат вредных веществ, таких как кадмий, и поэтому являются более экологически безопасными.
Щелочные аккумуляторы широко применяются в различных устройствах, таких как пульты дистанционного управления, игрушки, фотоаппараты и других портативных устройствах. Они также могут быть использованы в солнечных батареях, автомобильных аккумуляторах и других промышленных приложениях.
Описание щелочных аккумуляторов
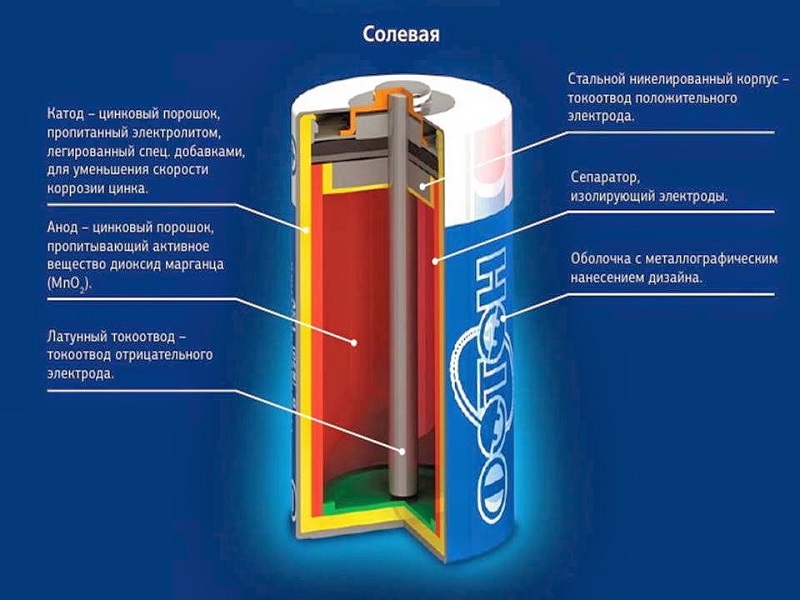
Щелочные аккумуляторы — это тип аккумуляторов, которые используют в качестве электролита щелочные растворы. Они характеризуются высоким уровнем энергии и долгим временем хранения заряда.
Одной из особенностей щелочных аккумуляторов является то, что они обладают низкой саморазрядкой, что означает, что они могут храниться в течение длительного времени без потери большой части своей емкости.
Щелочные аккумуляторы используют щелочные растворы, такие как гидроксид калия или гидроксид натрия, в качестве электролита. Эти растворы обеспечивают более стабильную работу аккумулятора и позволяют ему иметь высокий уровень энергии.
Щелочные аккумуляторы широко используются в различных устройствах, таких как фотоаппараты, игрушки, электронные устройства и другие. Они обычно имеют большую емкость и могут быстро заряжаться.
Одной из главных преимуществ щелочных аккумуляторов является их низкая стоимость и высокая эффективность. Они также очень удобны в использовании и обслуживании.
Щелочные аккумуляторы могут быть перезаряжаемыми и долговечными, что делает их более экологически безопасными и экономически выгодными в долгосрочной перспективе.
Принцип работы щелочных аккумуляторов
Щелочные аккумуляторы являются одним из наиболее распространенных типов аккумуляторов, используемых в различных электронных устройствах. Они основываются на принципе химической реакции, происходящей внутри аккумулятора и обеспечивающей его работу.
В состав щелочного аккумулятора входят два основных электрода — анод и катод, а также электролит, который служит средой для перемещения ионов между электродами.
Процесс зарядки щелочного аккумулятора начинается с того, что внешнее электрическое напряжение подается на аккумулятор. Под воздействием этого напряжения, на аноде аккумулятора происходит окисление, в результате которого образуются гидроксиды никеля и кадмия.
Когда аккумулятор используется и ток начинает протекать через него, гидроксиды никеля и кадмия растворяются, образуя оксиды никеля и кадмия. Эти оксиды переносятся в электролит и одновременно основание (кислотные ионты) передаются на катод, где происходит процесс восстановления оксидов кадмия и никеля в их первоначальные гидроксиды.
Таким образом, при работе аккумулятора происходит перекисание химической энергии в электрическую. Для обратного процесса, то есть зарядки аккумулятора, внешнее электрическое напряжение подается в обратном направлении, и процессы на электродах инвертируются.
Литий-ионные аккумуляторы
Литий-ионные аккумуляторы являются одними из самых популярных типов аккумуляторов в современных электронных устройствах. Они широко используются в смартфонах, ноутбуках, планшетах и других портативных устройствах. Главная особенность литий-ионных аккумуляторов заключается в том, что они способны сохранять большую емкость при небольшом весе и размерах.
Структура литий-ионного аккумулятора состоит из двух электродов: положительного и отрицательного, разделенных электролитом. Положительный электрод обычно состоит из лигированного оксида лития, а отрицательный — из углеродного вещества, например, графита. В процессе разряда аккумулятора литийионы перемещаются из положительного электрода в отрицательный через электролит. При зарядке процесс происходит в обратном направлении.
Сравнительно невысокий шоковый и тепловой разрыв напряжения является еще одним преимуществом литий-ионных аккумуляторов. Однако, они не защищены от перегрузки и перезарядки, поэтому использование специального контроллера зарядки для запаски энергии имеет важное значение. Кроме того, литий-ионные аккумуляторы могут саморазряживаться со временем, что обычно происходит в течение нескольких лет после начала их эксплуатации, поэтому периодическая замена аккумулятора является необходимой процедурой.
В зависимости от конструкции и химической составляющей, литий-ионные аккумуляторы могут иметь различные характеристики, такие как емкость, напряжение и ток разряда. Это позволяет использовать их в различных типах электронных устройств, обеспечивая энергией их работу на длительное время. Важно соблюдать правила эксплуатации и хранения литий-ионных аккумуляторов, чтобы избежать поломок и повреждений, а также продлить их жизненный цикл.
Описание литий-ионных аккумуляторов
Литий-ионные аккумуляторы являются одними из самых популярных аккумуляторов в современных устройствах. Они обладают высокой энергетической плотностью и способны хранить большое количество энергии. Кроме того, литий-ионные аккумуляторы отличаются небольшим размером и легким весом, что делает их идеальным выбором для мобильных устройств.
Основой литий-ионных аккумуляторов является реакция между литием и ионами, которая происходит внутри аккумулятора. Аккумулятор состоит из двух электродов — катода и анода, разделенных электролитом. Процесс зарядки и разрядки аккумулятора происходит благодаря перемещению литиевых ионов между электродами.
Катодом в литий-ионных аккумуляторах чаще всего является оксид металла, такой как оксид лития. Анодом же служит графитовый слой, который способен вступать в реакцию с литием и образовывать соединение LiC6. В результате процесса зарядки аккумулятора, литиевые ионы перемещаются с анода на катод через электролит, восстанавливая оксид металла. Во время разрядки аккумулятора, происходит обратная реакция — литиевые ионы перемещаются с катода на анод, восстанавливая графитовый слой.
Литий-ионные аккумуляторы имеют множество преимуществ перед другими типами аккумуляторов. Они не требуют обслуживания, не имеют эффекта памяти, обладают высоким КПД и долгим сроком службы. Кроме того, литий-ионные аккумуляторы являются экологически безопасными, так как не содержат вредных веществ, таких как свинец или кадмий.
Принцип работы литий-ионных аккумуляторов
Литий-ионные аккумуляторы — это тип аккумуляторов, основанных на литии-ионном химическом процессе. Они широко используются в различных устройствах, таких как смартфоны, планшеты, ноутбуки и электромобили.
Принцип работы литий-ионного аккумулятора основан на движении ионов лития между различными слоями электродов. Аккумулятор состоит из двух электродов — катода и анода, которые погружены в электролит — среду, способную проводить ионы. Катод обычно изготавливается из оксида лития-кобальта, а анод — из графита.
При зарядке аккумулятора, литий-ионы перемещаются из катода в анод через электролит. Это происходит благодаря электрической силе притяжения между полярными областями электродов. Литий-ионы встречаются с графитовыми слоями анода и встраиваются в их структуру.
Во время разряда аккумулятора происходит обратный процесс — ионы лития перемещаются из графитового анода в катод, освобождая энергию, которая приводит в движение электрические устройства.
Преимущества литий-ионных аккумуляторов включают высокую энергетическую плотность, низкую саморазрядку, отсутствие эффекта памяти и быструю зарядку. Однако они также имеют ограниченный срок службы и подвержены взрыву и пожару при неправильном использовании или дефектах.
Никель-кадмиевые аккумуляторы
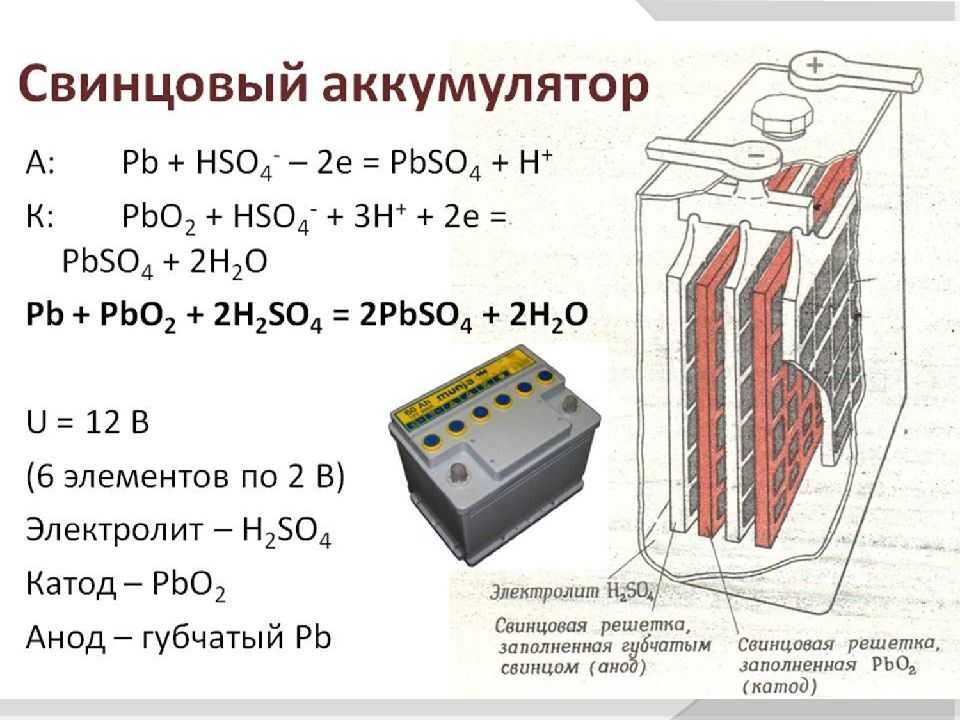
Никель-кадмиевые аккумуляторы — это тип аккумуляторов, использующих никель и кадмий в качестве активных материалов. Они широко применяются в различных устройствах, таких как мобильные телефоны, камеры, ноутбуки и другие электронные устройства.
Одной из особенностей никель-кадмиевых аккумуляторов является их высокая плотность энергии. Это означает, что они способны хранить большее количество электрической энергии на единицу массы по сравнению с некоторыми другими типами аккумуляторов.
Никель-кадмиевые аккумуляторы также обладают высокой степенью перезаряжаемости, что позволяет им быть использованными многократно. Они могут быть перезаряжены сотни раз без потери своих характеристик. Кроме того, они обладают низким саморазрядом, что означает, что они будут долго сохранять свою зарядку даже при хранении.
Однако никель-кадмиевые аккумуляторы обладают и некоторыми недостатками. Они имеют относительно низкую рабочую температуру и, следовательно, не могут быть использованы в экстремальных условиях. Также они имеют побочные продукты, такие как кадмий и водород, которые являются вредными для окружающей среды и требуют специальной обработки при утилизации.
В целом, никель-кадмиевые аккумуляторы являются надежным и эффективным источником энергии, который широко применяется в различных сферах жизни. Однако, из-за своих недостатков, на замену им приходят другие типы аккумуляторов, такие как литий-ионные и литий-полимерные, которые обладают более высокой энергоемкостью и безопасностью.
Описание никель-кадмиевых аккумуляторов
Никель-кадмиевые аккумуляторы являются одним из видов перезаряжаемых аккумуляторов, которые используются во множестве устройств, начиная от мобильных телефонов и заканчивая электрическими автомобилями. Они были разработаны в 20-х годах XX века и до сих пор остаются популярными из-за своей высокой энергетической плотности.
Основными компонентами никель-кадмиевых аккумуляторов являются два электрода: катод и анод. Катодом служит пластина, покрытая кадмием, а анодом — пластина из никеля. Между ними находится электролит, который обеспечивает перенос зарядов между электродами.
Принцип работы никель-кадмиевых аккумуляторов основан на химической реакции между кадмием и никелем. При разряде аккумулятора, кадмий окисляется, передавая электроны аноду, сам же преобразуясь в ион кадмия. В то же время, никель проходит процесс редукции, поглощая электроны и превращаясь в ион никеля. Эта реакция обратима, поэтому аккумуляторы могут быть перезаряжены и снова использованы.
Никель-кадмиевые аккумуляторы отличаются высокой энергоемкостью и способностью выдавать высокие токи. Они также обладают низким эффектом памяти, что позволяет заряжать их в любой момент без необходимости полного разряда. Однако стоит отметить, что никель-кадмиевые аккумуляторы имеют небольшую жизненную продолжительность и требуют специального зарядного устройства.
Принцип работы никель-кадмиевых аккумуляторов
Никель-кадмиевые аккумуляторы широко используются в различных устройствах, таких как портативные электронные устройства, инструменты, электромобили и другие. Принцип работы никель-кадмиевых аккумуляторов основан на химической реакции между никелевыми и кадмиевыми электродами, а также на движении ионов в электролите.
Внутри аккумулятора имеется два электрода — никелевый и кадмиевый, которые погружены в электролит. Кадмиевый электрод является отрицательным, никелевый — положительным. При подключении аккумулятора к источнику электрического тока, начинается химическая реакция между электродами.
Во время разряда аккумулятора, кадмиевый электрод окисляется, а никелевый электрод проявляет свойство восстанавливаться. Кадмий превращается в гидроокись кадмия (Cd(OH)2), а никелевый электрод окисляется, превращаясь в никелевый гидрооксид (NiOOH).
Во время зарядки аккумулятора, происходит обратная химическая реакция. Под действием внешнего источника электрического тока, гидроокись кадмия превращается в кадмий, а никелевый гидрооксид окисляется, образуя никель. Это позволяет аккумулятору сохранить электрическую энергию, которая затем может быть использована в устройстве, к которому аккумулятор подключен.